2026年3月27日,我校教师在中国科学院(2025年)1区TOP期刊《Materials Today Bio》(IF 10.2)上发表题为“An engineered ROS-responsive cascade nanoplatform delays Alzheimer's disease progression via Nrf2/GPX4-mediated microglial functional reprogramming”的最新研究成果 (https://doi.org/10.1016/j.mtbio.2026.103055)。

阿尔茨海默病(AD)的发生与发展由高度耦合的病理网络驱动,其中小胶质细胞介导的神经炎症、氧化应激与脑内铁代谢紊乱相互关联、相互促进。持续异常激活的小胶质细胞不仅是这一病理级联反应的关键驱动因素,同时也使小胶质细胞自身易受铁过载诱导的氧化损伤与铁死亡影响。因此,在AD进展过程中,小胶质细胞既是核心调控者,也是病理损伤的受害者。开发能够穿越血脑屏障、并对这一以小胶质细胞为核心的调控枢纽进行精准干预的纳米治疗策略,仍是当前面临的重大挑战。
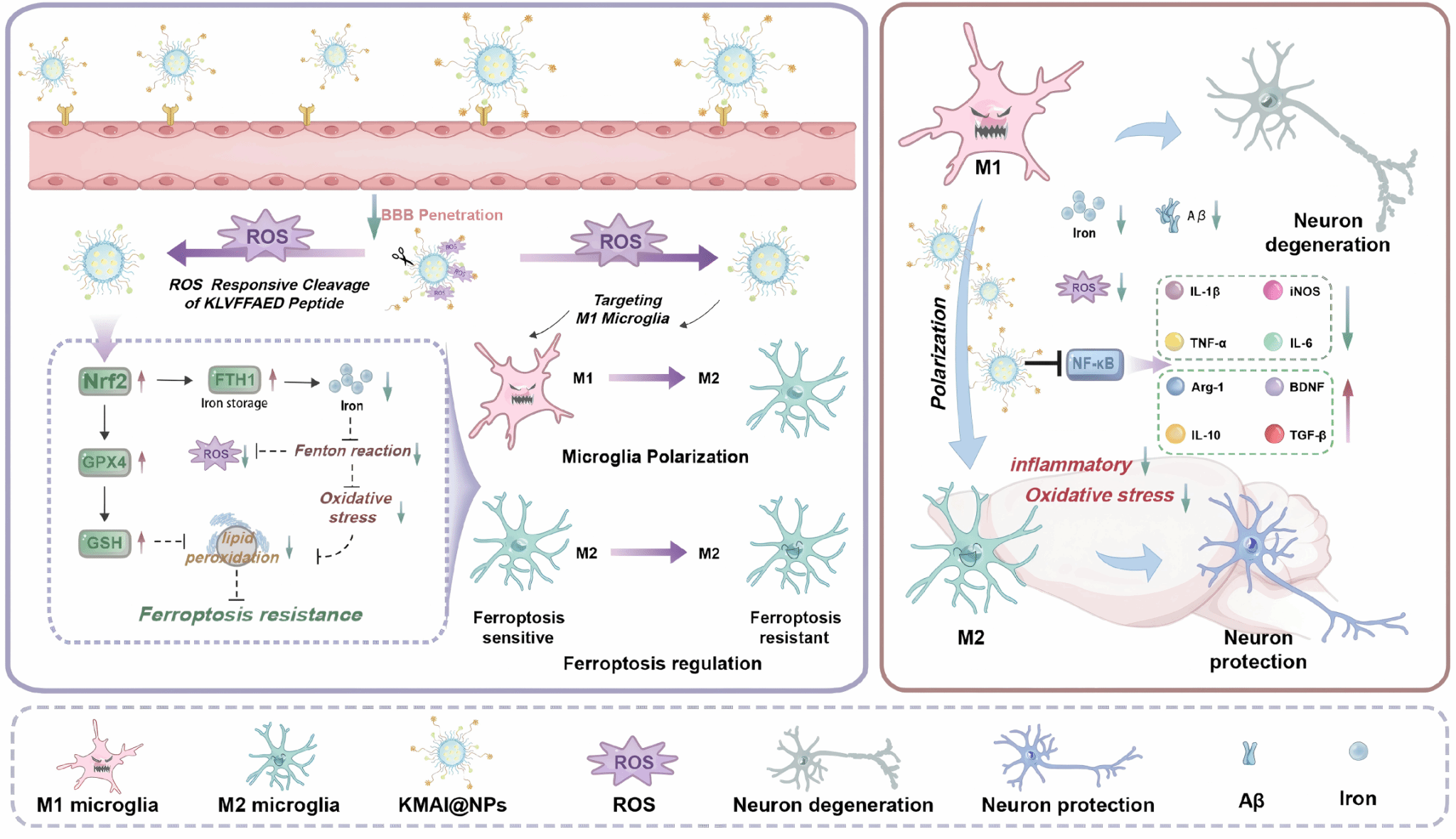
针对上述治疗困境,该研究构建了一种工程化活性氧响应型级联靶向纳米平台(KMAI@NPs)。该平台以乙酰水杨酸改性葡聚糖自组装为基础,进一步整合多肽靶向模块,实现长循环、高效血脑屏障穿透及活性氧触发的级联靶向。该研究系统优化了葡聚糖分子量及乙酰水杨酸的接枝率,实现了对纳米平台自组装行为与体内稳定性的理性调控。体内外研究证实,KMAI@NPs可有效重编程小胶质细胞功能状态,促进其向抗炎表型极化。值得注意的是,该研究表明:KMAI@NPs驱动的Nrf2激活对于缓解M2型小胶质细胞的铁死亡易感性至关重要,从而维持其免疫调节与神经保护功能。在AD小鼠模型中,给予KMAI@NPs可实现多维度病理协同改善,包括减轻神经炎症与氧化应激、减少β淀粉样蛋白沉积,并显著提升认知功能。该研究将中药活性成分、智能靶向纳米载体、小胶质细胞免疫调控三者深度融合,提出以小胶质细胞为核心枢纽的AD多靶点协同治疗新策略,为应对神经退行性疾病复杂病理网络提供了极具前景的新思路。